Salut Bio22,
die Struktur einer Aminosäure macht es ja möglich, dass sie sowohl als Brønsted - Säure als auch als Brønsted - Base reagieren kann. In wässriger Lösung treten Aminosäuren zumeist als Zwitterionen auf, d.h mit deprotonierter Carboxygruppe und protonierter Aminogruppe. Wird nun Säure zu einer Lösung hinzugefügt, die das Zwitterion enthält, fängt die Carboxygruppe ein Wasserstoffion (H+) ein und die Aminosäure wird positiv geladen. Wird hingegen eine Base hinzugefügt, entsteht durch die Entfernung des H+- Ions aus der Aminogruppe eine negativ geladene Aminosäure.
Als Zwitterion in wässriger Lösung stellt sich die Struktur von Alanin also folgendermaßen dar:
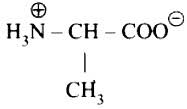
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
Die Struktur durch Hinzufügung von Säure oder Base:
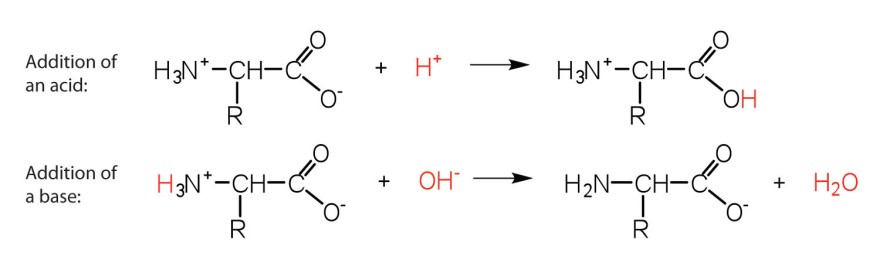
Letztere sind allgemeine Abbildungen. In Bezug auf Alanin tausche daher bitte jeweils "R" durch eine CH3 - Gruppe aus.
Schöne Grüße :)