Grüße chemweazle,
Ether Synthese und Lösungsmittel
Aufgabe:
Nr.1 Als Lösungsmittel zur Extraktion von ätherischen Ölen aus Kräutern soll Dimethylether verwendet werden.
Ätherische Öle lösen sich nicht in Wasser. Erläutern Sie die Wirksamkeit dieses Verfahrens anhand des Baus der Dimethylether-Moleküle und deren zwischenmolekularen Kräfte.
Nr.2 Die Synthese von Diethylether kann aus Ethanol erfolgen. Dazu wird konzentrierte Schwefelsäure als Katalysator eingesetzt. Formulieren Sie eine Reaktionsgleichung zur Synthese von Diethylether.
Nr.3 Formulieren Sie den Reaktionsmechanismus für die in Aufgabe 2 der genannten Synthese.
Problem/Ansatz:
Nr.1
Ether-Moleküle sind schwache Dipole, können aber keine Wasserstoffbrücken ausbilden, daher ist ihre Wasserlöslichkeit gering.
Ätherische Öle bestehen hauptsächlich aus lipophilen Verbindungen.
Das ist alles was ich dazu weiß.
Ether-Moleküle haben 2 schwache, polare Kohlen-Sauerstoff-Bindungen, die zueinander noch gewinkelt sind.
Die Polarität nach außen hin ist jedoch sehr sehr schwach gegenüber ihrer Lipophilie.
Ether sind deshalb lipophile Lösungsmittel wie z.B.: Pentan, Chloroform, Dichlormethan, Benzen, Toluen etc.
Sie eignen sich deshalb zur Extraktion überwiegend lipophiler Pflanzenwirkstoffe.
Löslichkeit lipophiler Substanzen in Diethylether
Viele lipophile Substanzen, darunter Fette, die Terpene und sonstige Naturstoffe haben Moleküle mit aneinander gereihten Ringen und oder verzweigten Kettenteilen.
Geraten nun Diethylether-Moleküle und solche lipophile Substanzen in kurzen Abständen in die Nähe, so wirken zwischen den Ringen und verzweigten Kohlenstoff-Ketten und den C2H5-Gruppen der Diethylether-Moleküle die sog. Van der Waalschen-Anziehungs-Kräfte, die Diethylether-Moleküle und diese o.g. lipophilen Moleküle reißen sich aneinander und bilden Gemische(Lösungen)
Nr.2
2 C2H5OH → C2H5-O-C2H5 + H2O
Auf dem Reaktionspfeil habe ich H2SO4 stehen, da Schwefelsäure ja der Katalysator ist.
Ist die Reaktion so richtig und könnte mir die jemand genauer erklären?
Prima, sehr gut, das ist richtig, man setzt den Katalysator noch in runde Klammern, um ihn von den Reaktionsteilnehmern, zu unterscheiden.
Die Ausgangsstoffe werden bei einer Reaktion zum Teil, oder fast vollständig, verbraucht, der Katalysator wird entweder im Laufe der Reaktion oder spätestens am Ende der Reaktion wieder freigesetzt und liegt am Ende unverändert vor.
Deshalb wird der Kat. in runde Klammern gesetzt.
Bildchen 1
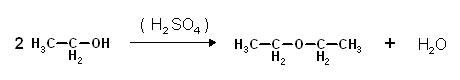
Da diese Reaktion auch prizipiell umkehrbar ist, trotz der sehr sehr geringen Löslichkeit des Diethylethers in Wasser oder wäßriger, verdünnter Schwefelsäure, kann man auch den Harpunen-Pfeil oder Doppelpfeil anstelle des einfachen Pfeils nach rechts verwenden.
Bildchen 2
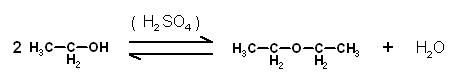
Auch läßt sich Diethylether mit wäßriger Schwefelsäurelösung wieder mit dem Wasser zu Ethanol hydrolysieren, mit Säure katalysierte Etherspaltung.
Nr.3
Reaktionsmechanismus
Reaktionsmechanismus zur Ethersynthese aus den entpr. Alkoholen durch Wasserabspaltung über Carbeniumionen, als Zwischenstufen
Hinweise zu den Alkyloxoniumionen und Dialkyloxoniumionen
Wassermoleküle lassen sich jeweils am freien Elektronen des Sauerstoffatoms durch starke, mittelstarke und schwache Säuren protonieren, dabei enstehen die Hydroniumionen oder Hydroxoniumionen, H3O(+) .
H2O + H(+)(aq) + X(-)(aq) ⇌ H3O(+)(aq) + X(-)(aq)
Ebenso ist das freie Elektronenpaar eines Sauertoffatoms der OH-Gruppe eines Alkohols protonierbar, dabei entsteht das Alkyloxoniumion, R-OH2(+) .
R-OH + H(+)(aq) + X(-)(aq) ⇌ R-OH2(+)(aq) + X(-)(aq)
Das gilt auch für Ethermoleküle, hier werden Di-Alkyl-Oxoniumionen gebildet.
R2O + H(+)(aq) + X(-)(aq) ⇌ R2OH(+)(aq) + X(-)(aq)
Reaktionsmechanismus am Beispiel von Diethylether
1.
Hinreaktion
Protonierung des Alkohols durch die Säure(Schwefelsäure) zum Alkyl-Oxoniumsalz mit dem Alkyl-Oxoniumion und dem Hydrogensulfation als Gegenion
CH3-CH2-OH + H2SO4 ⇌ CH3-CH2-OH2(+) + HSO4(-)
Rückreaktion
Deprotonierung des Ethyl-Oxoniumions
2.
Hinreaktion
Carbeniumionen-Bildung durch Wasserabspaltung(Eliminierung) an den Alkyloxoniumionen der Alkyloxoniumsalze
Das Wassermolekül ist die Abgangsgruppe, das Nucleofug, am protonierten Alkohol(Alkyloxoniumion).
CH3-CH2-OH2(+) + HSO4(-) ⇌ CH3-CH2(+) + HSO4(-) + H2O
Rückreaktion
Nucleophile Addition des Wassermoleküls mit dem freien Elektronenpaar an das elektrophile Ethylkation(Carbeniumion)
Carbeniumionen: Aus Ethanol wird das Ethyl-Kation und aus Methanol das Methyl-Kation gebildet.
3.
Hinreaktion
Nucleophile Addition der OH-Gruppen der Alkohole mit den freien Elektronenpaaren an die Carbeniumionen(Elektrophile) unter Ausbildung von Di-Alkyl-Oxoniumsalzen (am Sauerstoffatom protonierte Ethermoleküle, positiv geladen mit Hydrogensulfationen als Gegenionen)
CH3-CH2(+) + HSO4(-) + HO-CH2-CH3 ⇌ CH3-CH2-O(+)-CH2-CH3 + HSO4(-)
Rückreaktion
Dissoziation, Austritt der Alkohol-Moleküle als Abgangsgruppen, das ist die Rückbildung der Alkyl-Kationen(Ethyl-Kationen, Carbeniumionen)
4. Deprotonierung der Di-Alkyl-Oxoniumsalze zum Dialkylether
Hinreaktion
CH3-CH2-O(+)-CH2-CH3 + HSO4(-) ⇌ CH3-CH2-O-CH2-CH3 + H(+) + HSO4(-)
Rückreaktion
Protonierung der Sauerstoff-Atome am freien Elektronenpaar
Skizze 1
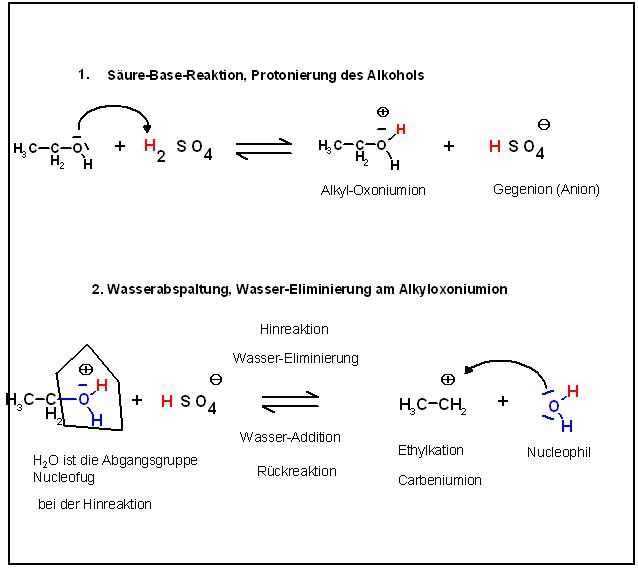
Skizze 2