Aufgabe:
Brauche Hilfe bei den Oxidationszahlen von Natriumdichromat
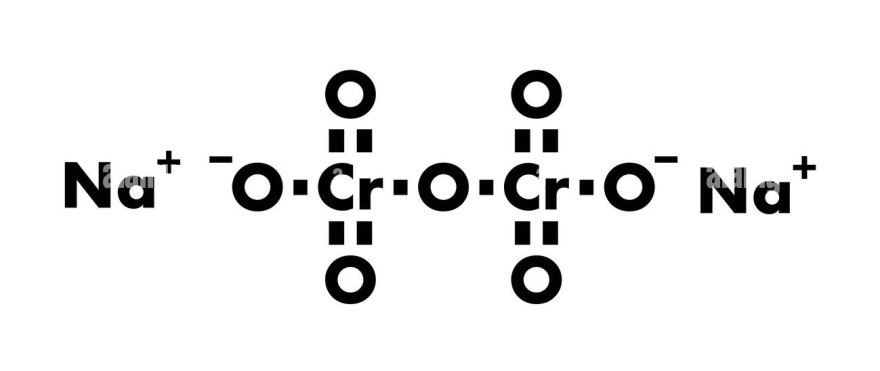
Problem/Ansatz:
Natrium hat die Oxidationszahl +I.
Sauerstoff hat die Oxidationszahl -II.
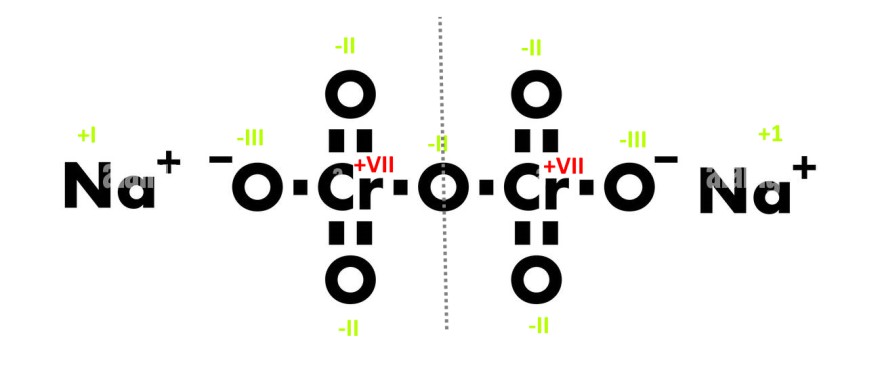
Die einfach negativen Sauerstoff haben dann die Oxidationzahl -III
Das Sauerstoff in der Mitte wird halbiert, also für jedes Chrom nochmal -I auszugleichen.
Somit sind in der Summe -8 um jedes Chrom-Atom. Aber da wir ja 2 Natrium Atome haben, die einfach positiv sind, und das Molekül insgesamt elektrisch neutral ist, gelten dann -7 pro Chrom-Atom.
Also muss Chrom eine Wertigkeit von +VII haben.
Aber in meinem Periodensystem (Wolfenthal) hat Chrom keine Wertigkeit von 7, nur Mangan.