Aufgabe:
Warum trägt das Stickstoff in der Nitrogruppe eine positive Ladung?
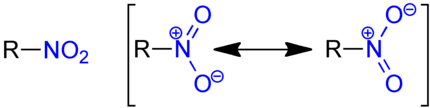
Problem/Ansatz:
Ich verstehe das nicht, Stickstoff hat doch so viele verschiedene Wertigkeiten (5,4,3,2), warum sucht es sich nicht einfach eine W aus, wo es Neutral geladen ist.