Salut,
Begründen Sie anhand des MO-Schemas für Neon, warum es keine Ne2-Molekühle gibt.
Elektronenkonfiguration Ne: 1s2 2s2 2p6
Neon hat also 8 Valenzelektronen und da wir für ein theoretisches Ne2 - Molekül 2 x das Element benötigen, haben wir 16 Valenzelektronen.
Das MO - Schema für Neon sieht nun folgendermaßen aus, wobei ich jetzt voraussetzen muss, dass du mit der erforderlichen Schreibweise bzw. dem Aufbau vertraut bist:
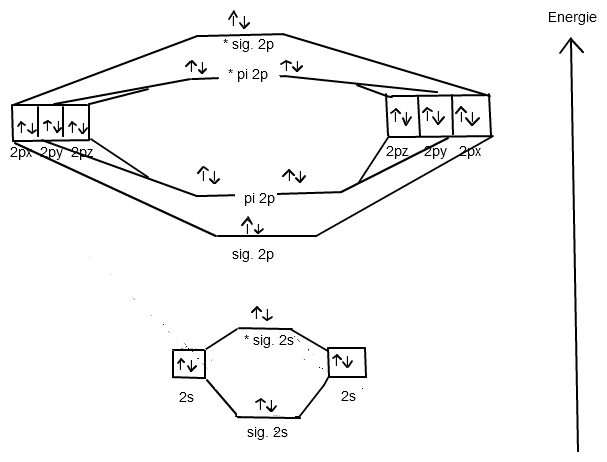
Daraus kannst du jetzt gemäß folgender Formel die Bindungsordnung BO bestimmen:
1/2 * (bindende Valenzelektronen - antibindende Valenzelektronen)
(Ganz ausführlich: σ 2s (2e-) + σ 2p (2e-) + π 2p (4e-) - *σ 2s (2e-) + *π 2p (4e-) + *σ 2p (2e-)
BO = 1/2 * (8 bindende Valenzelektronen - 8 antibindende Valenzlektronen) = 0
Ist die Bindungsordnung 0, so resultiert daraus, dass ein Ne2 - Molekül nicht existiert.
Schöne Grüße :)