Additionsreaktionen an 1-Ethylcyclohexen
Darstellung des 1-Ethylcyclohexens
Retrosynthetischer Weg
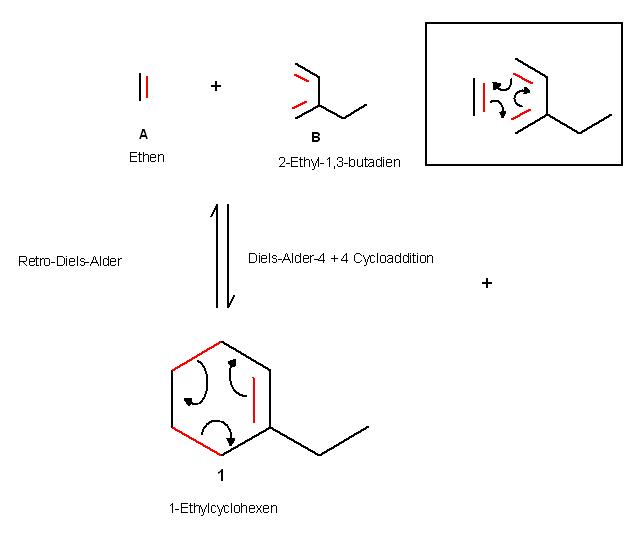
Die Retro-Diels-Alder-Reaktion, die Umkehr-Reaktion zur Diels-Alder 2 + 4 –Cycloaddition, liefert Ethen und 2-Ethyl-1,3-Butadien.
Diese Umkehrreaktion, die Retro-Diels-Alder-Reaktion wird auch Cycloreversion genannt, da es sich um eine Ringöffnung handelt.
Die Diels-Alder (4 +2) – Cycloaddition ist eine reversible Reaktion.
Umgekehrt führt die (4 + 2) - Cycloaddition (Diels-Alder-Cyclisierung) von Ethen, A, und dem 2-Ethyl-1,3-Butadien zum Produkt 1, dem 1-Ethylcyclohexen.
Die Zahl 2 steht für die beiden C-Atome im Ethen und die Zahl 4 steht für die Anzahl der C-Atome im Butadien-gerüst, ohne Berücksichtigung von weiteren Substituenten.
Aus diesen 2 C-Atomen des Alkens plus den 4 C-Atomen des Alkadiens wird der Sechsring mit einer einzigen Doppelbindung gebildet. Es st das Cyclohexengerüst.
Skizze
Bem. zu den Additionsreaktionen
Es gibt hier 2 Typen von Additionen, es sind die syn-Additionen und die anti-Additionen.
Es gibt die syn-Additionen wobei die beiden Addenden gleichzeitig nur von einer Seite an die Kohlenstoffatome der C-C-Doppelbindung addiert werden.
Reaktionen von 1 mit KMnO4 / H2O (syn-Hydroxylierung) zu D und mit D2 / Pd zu F ( syn-Addition von Wasserstoff, hier das Wasserstoffisotop Deuterium , auch syn-Hydrierung genannt
Bei cyclo-Alkenen führen die syn-Additionen zu cis-Diastereomeren, cis-Formen der Additionsprodukte.
Wenn man die Ausrichtung des Cycloalkens 1 so beibehält wie in der Skizze angegeben, so kann einmal eine syn-Addition von z.B. 2 OH-Gruppen oder 2 H-Atomen entweder unterhalb der Zeichenebene oder oberhalb der Zeichenebene erfolgen.
In Lösung findet die syn-Addition bei der einen Hälfte der Molekühlanzahl von der einen Seite und bei der anderen Hälfte der Moleküle werden die Addenden von der anderen Seite der Doppelbindung addiert.
Das führt zu bild- und spiegelbild-isomeren Addukten(Produkte), Enantiomere.
Stereochemische Aspekte
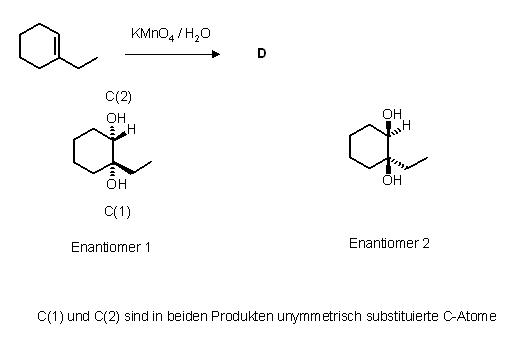
1 (1-Ethylcyclohexen) + KMnO4 / H2O → D
Bei der syn-Addition von 2 OH-Gruppen an die C-C-Doppelbindung des Edukts 1, dem 1-Ethylcyclohexen,werden 2 (Enantiomere) 1,2-Diole (Glycole) gebildet.
Beim dem einen Isomer(Enantiomer) stehen die beiden OH-Gruppen im Produkt oberhalb der Zeichenebene das H-Atom an C-Atom Nr. 2 und der Ethylrest an C-Atom Nr. 1 zeigen unterhalb der Zeichenebene.
Bei dem anderen Enantiomer wurden die beiden OH-Gruppen von unten an die C-C-Doppelbindung addiert.
Hier stehen beide OH-Gruppen in cis-Stellung unterhalb der Zeichenebene, der Ethylrest an C(1) und das Wasserstoffatom an C(2) stehen bei diesem Isomer oberhalb der Ebene.
Die beiden Isomere unterscheiden sich in den Konfigurationen an den Atomen C(1) und C(2).
Es sind Enantiomere. Dreht man eines der beiden Produktmoleküle um eine Achse in der Zeichenebene um 180 Grad so zeigt sich das Spiegelbild zum anderen.
Es liegt eine Bild-Spiegelbild-Isomerie vor. (Enantiomerie)
Skizze zur syn-Hydroxylierung von 1(1-Ethylcyclohexen)
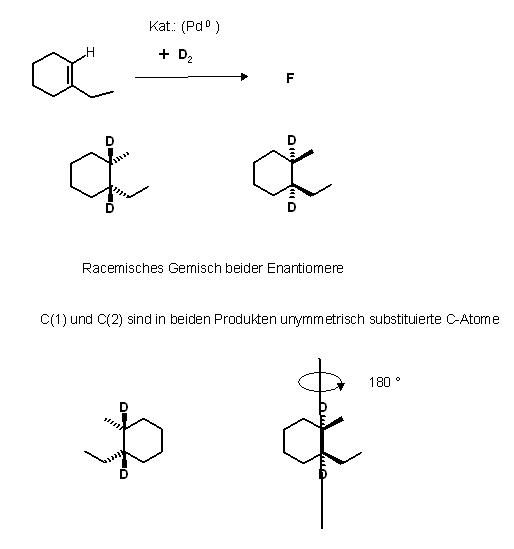
Die Katalytische syn-Hydrierung, die syn-Deuterierung mit elementaren Deuterium (Wasserstoffisotop) führt zu 2 cis-Addukten. Die beiden Deuteriumatome stehen immer in cis- Position zueinander.
Und auch diese syn-Addition erfolgt bei einem Teil der Edukt-Moleküle von oben und bei einer gleichgroßen Anzahl der Moleküle von der entgegengesetzten Seite, von unten..
Dadurch entstehen zueinander spiegelbildliche Addukte, Enantiomere.
Skizze zur Katalytischen syn Hydrierung(Deuterierung) von 1
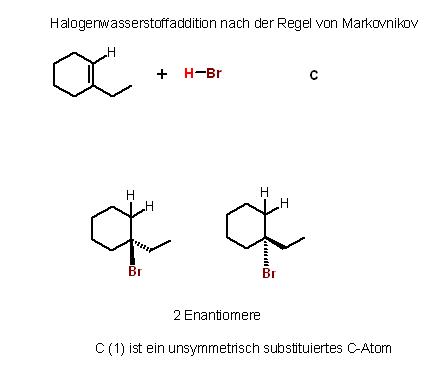
Einschub: Die Bromwassertoff-Addition an das Alken 1, 1-Ethylcyclohexen
1 + H-Br → C
Die Addition verläuft sicherlich nach der Regel von Markovnikov.
Bromwasserstoff addiert sich mit dem H-Atom an das C-Atom der C-C-Doppelbindung mit den meisten H-Atomen, also an das Atom C(2), denn das trägt 1 H-Atom, C(1) trägt kein H-Atom, dort befindet sich der Ethylrest.
Das Bromatom wird nach Markovnikov an C(1) addiert.
Es gibt 2 Addukte, 2 Enatiomere, Bild-Spiegelbild-Isomere.
Einmal wird das Br-Atom von oben an C(1) addiert, bei einen anderen Teil der Moleküle erfolgt die Addition der Bromatome an C(1) von unten her.
Bei beiden Produkten sind die C-Atome C(1) jeweils unsymmetrisch substituiert.
Und jedes der beiden Produkte hat nur ein einziges unsymmetrisch substituiertes c-Atom.
Die Konfigurationen an C(1) sind bei beiden Produkten spiegelbildlich.
Das Produkt ist chiral. Es liegt ein 1 zu 1-Gemisch zweier Enatiomere vor, das ist ein Racemat.
Skizze :1-Ethylcyclohexen HBr-Addition, Markovnikov-Produkt
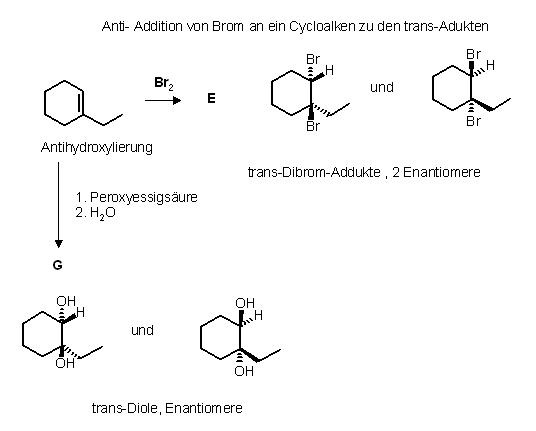
Anti-Additionen an Edukt 1 , 1-Ethylcyclohexen
Anti-Bromaddition
1 + Br2 → E/p>
Anti-Hydroxylierung mit Peroxocarbonsäure und Wasser
Edukt 1 + 1. Peroxyessigsäure , 2. H2O → G
SKizze